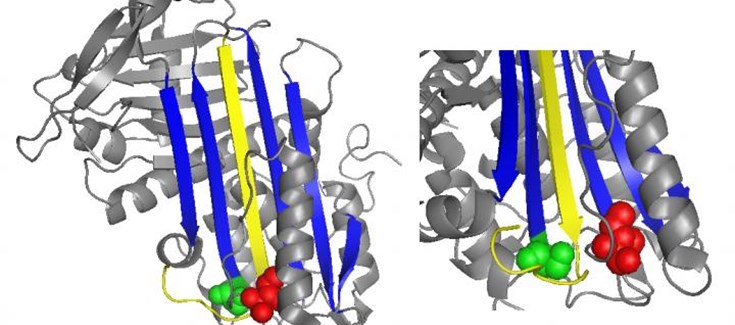
Un estudio realizado por investigadores de la U765 CIBERER que lidera el Dr. Vicente Vicente en el Instituto Murciano de Investigación Biosanitaria ha identificado en pacientes con trombosis nuevas mutaciones en el principal anticoagulante endógeno, la antitrombina, que provocan la deficiencia de antitrombina, una enfermedad hereditaria caracterizada por un elevado riesgo de sufrir trombosis.
Esta mejor comprensión del funcionamiento de la antitrombina podría ayudar a conseguir tratamientos más adecuados no solo para pacientes con esta enfermedad rara que afecta a una de cada 5.000 personas sino también para todos los pacientes con trombosis (1/1.000 sujetos cada año).
La coagulación es esencial para evitar la muerte por hemorragia ante cualquier herida. Sin embargo, una vez el peligro ha pasado es también esencial frenar la respuesta de coagulación para prevenir las trombosis (obstrucción del flujo sanguíneo por coágulos). Una proteína llamada antitrombina es la encargada de controlar adecuadamente la coagulación. Los afectados por la deficiencia de antitrombina tienen un riesgo mucho mayor de sufrir trombosis que incluso puede poner en peligro su vida.
Este estudio, coordinado por el Dr. Javier Corral, investigador de la U765, ha analizado las mutaciones en la proteína antitrombina en afectados por esta enfermedad y ha descubierto que una zona de esta proteína tiene un papel en la inhibición de la trombina que era hasta ahora desconocido.
Hasta la fecha se pensaba que solo los residuos localizados en la región de la antitrombina que interacciona con la trombina eran cruciales en su mecanismo inhibitorio. Sin embargo, mediante una original aproximación que parte de los resultados obtenidos del estudio de pacientes, complementados con estudios de las variantes recombinantes, se ha identificado una nueva zona de este anticoagulante clave en el proceso inhibitorio. Los resultados de este trabajo se han publicado en el Journal of Biological Chemistry.
"El estudio de mutaciones identificadas en la naturaleza, en pacientes con una enfermedad rara, nos ha permitido conocer aspectos básicos de la actividad de este potente anticoagulante, extrapolables a otras moléculas similares, las serpinas, y abre nuevas perspectivas terapéuticas no solo para estos pacientes, sino para toda la patología trombótica e incluso otras serpinopatias”, explican los autores del artículo.
Este trabajo ha sido posible gracias a la caracterización de mutaciones identificadas en afectados por deficiencia de antitrombina. La U765 es un centro de referencia para el diagnóstico de la deficiencia de antitrombina. Desde hace 15 años, los investigadores de este laboratorio reciben muestras de pacientes con diversas mutaciones que afectan al funcionamiento de la antitrombina.
En el estudio, también han participado investigadores de la Universidad de Illinois en Chicago.
Disease-causing mutations in the serpin antithrombin reveal a key domain critical for inhibiting protease activities. Sonia Águila, Gonzalo Izaguirre, Irene Martinez-Martinez, Vicente Vicente, Steven T Olson and Javier Corral. Journal of Biological Chemistry.