Un estudio liderado por Ana Guadaño, jefa de grupo de la U708 CIBERER en el Instituto de Investigaciones Biomédicas “Alberto Sols” (CSIC-UAM), ha presentado los primeros resultados sobre la administración intranasal de hormonas tiroideas en modelos de ratón para intentar paliar las alteraciones neurológicas del síndrome de Allan-Herndon-Dudley.
Estos resultados, publicados en PLOS ONE, constituyen un primer paso para continuar en el estudio de esta vía de administración como potencial herramienta terapéutica para el síndrome de Allan-Herndon-Dudley, una enfermedad rara causada por mutaciones en un transportador de hormonas tiroideas denominado MCT8. Los pacientes presentan un grave retraso del desarrollo, discapacidad intelectual severa con falta de lenguaje y trastornos del movimiento.
Los problemas neurológicos de los pacientes son causados por una falta de entrada de hormonas tiroideas (T4 y T3) al cerebro (hipotiroidismo cerebral), ya que el transportador MCT8 se expresa abundantemente en la barrera hematoencefálica. Las mutaciones que inactivan esta proteína suponen un impedimento para que las hormonas tiroideas puedan atravesar esta barrera y llegar al cerebro. Al mismo tiempo la T3 se acumula en otros tejidos (hipertiroidismo periférico) dando lugar también a importantes alteraciones musculares y metabólicas.
La U708 CIBERER, en colaboración con grupos españoles, británicos y norteamericanos, ha probado por primera vez la administración de hormonas tiroideas por vía intranasal para tratar el síndrome de Allan-Herndon-Dudley en animales modelo de la enfermedad. Esta vía de administración supone una ruta directa al cerebro, evitando el paso a través de la barrera hematoencefálica.
En el estudio, los ratones deficientes del transportador MCT8 han sido tratados con diferentes formulaciones que contienen hormonas tiroideas con el objetivo de hacerla llegar directamente al cerebro y comprobar su eficacia.
Con las formulaciones administradas hasta ahora, la hormona se distribuía preferentemente por el torrente sanguíneo, empeorando la situación de hipotiroidismo periférico presente en estos animales.
Este estudio es, por tanto, una primera aproximación para el establecimiento de una formulación adecuada que permita la acumulación de hormonas tiroideas en el interior del cerebro sin empeorar la situación de hipertiroidismo periférico que caracteriza también a esta enfermedad.
En la actualidad, no existe ningún tratamiento que sea capaz de mejorar las alteraciones neurológicas de estos pacientes. El grupo liderado por la Dra. Guadaño está centrado en el estudio de diferentes estrategias terapéuticas en animales deficientes del transportador MCT8 como modelo de la enfermedad con el objetivo de encontrar un potencial tratamiento para los pacientes de esta enfermedad rara. El equipo publicó recientemente otro trabajo en el que también usaban una vía de administración alternativa, a través del ventrículo cerebral, con el mismo objetivo de evitar el paso a través de la barrera hematoencefálica.
Los resultados obtenidos en estos trabajos aportan datos valiosos para seguir trabajando en el desarrollo de nuevas estrategias terapéuticas dirigidas a lograr un efecto directo en el cerebro de estos pacientes que sufren graves daños neurológicos desde edades muy tempranas y para los cuales no existe ninguna medida eficaz en la actualidad.
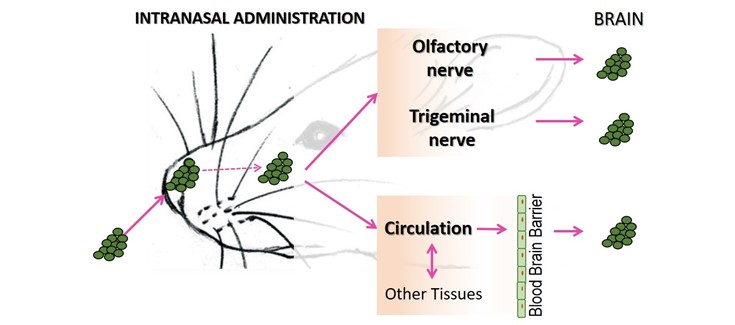
(*) Explicación de la figura: La administración de hormonas tiroideas a través de la cavidad nasal permite su entrada directa al cerebro, a través de la vía del nervio trigémino o del nervio olfativo, sin necesidad de atravesar la barrera hematoenfálica. A su vez, parte de las hormonas administradas pueden ir a la circulación sanguínea desde donde son transportadas al resto de tejidos, o al cerebro tras pasar la barrera hematoencefálica.
Artículo de referencia:
Intranasal delivery of Thyroid hormones in MCT8 deficiency. Carmen Grijota-Martínez, Soledad Bárez-López, Eva Ausó, Samuel Refetoff, William H Frey II, Ana Guadaño-Ferraz. PLOS ONE https://doi.org/10.1371/journal.pone.0236113