Investigadores de la U750 CIBERER que lidera Raúl Estévez en la UB-IDIBELL han participado en dos estudios publicados recientemente que demuestran la implicación de las proteínas LRRC8 en diferentes enfermedades raras: el síndrome de solo células de Sertoli (SCOS en sus siglas en inglés) y la leucoencefalopatía megalencefálica causada por mutaciones en los genes MLC1 o GLIALCAM.
Los canales de cloruro regulados por volumen formados por las proteínas LRRC8 tienen un papel clave en la regulación de volumen, la isquemia cerebral, la progresión del ciclo celular, la señalización por insulina y la resistencia tumoral a cisplatino. En la primera de las investigaciones relacionadas con el papel de estas proteínas en enfermedades humanas, realizada por investigadores de la U750 en colaboración con el grupo dirigido por Fernando Benavides (University of Texas, USA), se describe la implicación de estas proteínas en el desarrollo de las células germinales masculinas. En concreto, el grupo de investigación liderado por el Dr. Estévez ha caracterizado una mutación hipomórfica encontrada en el gen LRRC8A en un paciente con SCOS, un grupo de enfermedades raras de esterilidad caracterizadas por la ausencia de células germinales.
Por otro lado, en una investigación publicada en Neurobiology of Disease, la U750 CIBERER ha demostrado que la actividad de las proteínas LRRC8 también está disminuida en un tipo raro de leucodistrofia (enfermedad de la substancia blanca del cerebro) llamada leucoencefalopatia megalencefálica, que está causada por mutaciones en los genes MLC1 o GLIALCAM. La relación entre GlialCAM/MLC1 y las proteínas LRRC8 es indirecta y se sugiere que MlC1 modifica el estado de fosforilación de las proteínas LRRC8 a través de la vía de las ERKs. En este último trabajo, han colaborado también investigadores de la U730 CIBERER que lidera Virginia Nunes en el IDIBELL, del Istituto Superiore di Sanità de Roma y de la Universitat de Barcelona.
Deficient LRRC8A-dependent volume-regulated anion channel activity is associated with male infertility in mice. Bao J, Perez CJ, Kim J, Zhang H, Murphy CJ, Hamidi T, Jaubert J, Platt CD,Chou J, Deng M, Zhou MH, Huang Y, Gaitán-Peñas H, Guénet JL, Lin K, Lu Y, Chen T,Bedford MT, Dent SY, Richburg JH, Estévez R, Pan HL, Geha RS, Shi Q, Benavides F. JCI Insight. 2018 Aug 23;3(16). pii: 99767. doi: 10.1172/jci.insight.99767. [Epub ahead of print] PubMed PMID: 30135305
GlialCAM/MLC1 modulates LRRC8/VRAC currents in an indirect manner: Implications for megalencephalic leukoencephalopathy. Elorza-Vidal X, Sirisi S, Gaitán-Peñas H, Pérez-Rius C, Alonso-Gardón M,Armand-Ugón M, Lanciotti A, Brignone MS, Prat E, Nunes V, Ambrosini E, Gasull X, Estévez R. Neurobiology of Disease. 2018 Aug1;119:88-99. doi: 10.1016/j.nbd.2018.07.031. [Epub ahead of print] PubMed PMID:30076890.
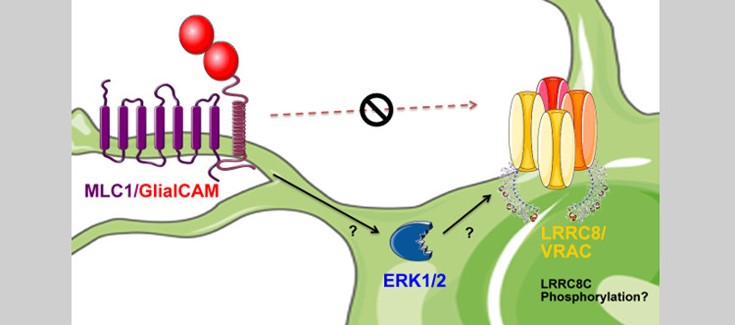
Pie de foto:
(*) La relación entre GlialCAM/MLC1 y las proteínas LRRC8 es indirecta y se sugiere que MlC1 modifica el estado de fosforilación de las proteínas LRRC8 a través de la vía de las ERKs.