
Investigadores de la U765 CIBERER que lidera Vicente Vicente en el Hospital Universitario Morales Meseguer de Murcia han estudiado las consecuencias bioquímicas y celulares de la mutación identificada en una extensa familia con deficiencia de antitrombina, el principal anticoagulante endógeno, que sufre una grave clínica trombótica, caracterizada por trombosis temprana y recurrente letal en la mayoría de los casos.
El fenotipo que presentaba esta familia llevó a realizar estudios adicionales a la caracterización molecular de dicha deficiencia. La mutación identificada en los pacientes afectaba al codón de inicio de la traducción (Met1) y justificaría totalmente la deficiencia, pero se evaluó su efecto en un modelo de expresión recombinante en células eucariotas. Como era de esperar, apenas se observaba antitrombina secretada en el medio de cultivo, validando los resultados observados en los pacientes. Pero sorprendentemente se detectaban altos niveles de expresión de dos tipos de antitrombina a nivel intracelular: una mayoritaria más pequeña que la silvestre, pero también expresaba antitrombina silvestre, que era la que se secretaba.
Javier Corral (U765 CIBERER), responsable de este trabajo publicado en Oncotarget, explica que cuando se elimina el codón AUG iniciador, el ribosoma continúa escaneando el RNA hasta encontrar un nuevo codón iniciador. El cambio genético que se observa de la secuenciación (Met1Ile en este caso) no tiene lugar, sino que la traducción comienza en la segunda metionina (49 residuos menos).
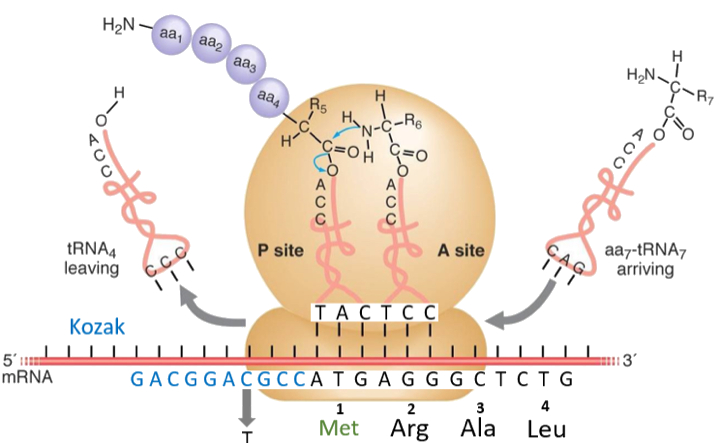
Los experimentos de José Navarro-Fernández y María Eugenia de la Morena-Barrio (investigadores también de la U765) confirmaron con estudios bioquímicos y de microscopia electrónica que como este residuo se localiza detrás del péptido señal, la cadena proteica no entra en el retículo endoplásmico, no se glicosila y tiene localización citoplasmática.
Este trabajo demuestra que las mutaciones que afectan al codón iniciador pueden generar proteínas más pequeñas, con distinta localización celular e incluso diferentes, que pueden adquirir nuevas funciones. Pero además, mediante multitud de mutagénesis dirigidas, este estudio demuestra que además del AUG que codifica metionina, todos los codones, excepto los stop, pueden servir de inicio de traducción en eucariotas.
“A veces la naturaleza, el estudio de pacientes con una patología, puede aportar información básica o extrapolable a otras muchas enfermedades”, destaca el Dr. Corral.
En la investigación, han colaborado investigadores de la Universidad de Murcia y el Hospital Universitario de Oslo (Noruega).
“Biochemical and cellular consequences of the antithrombin p.Met1? mutation identified in a severe thrombophilic family”. Navarro-Fernández J, Eugenia de la Morena-Barrio M, Martínez-Alonso E, Dybedal I, Toderici M, Bohdan N, Miñano A, Heimdal K, Abildgaard U, Martínez-Menárguez JÁ, Corral J, Vicente V. Oncotarget. 2018 Sep 4;9(69):33202-33214. doi: 10.18632/oncotarget.26059. eCollection 2018 Sep 4. PubMed PMID: 30237862; PubMed Central PMCID: PMC6145704.